Trong hóa học, bạn có gặp ký hiệu PT bao giờ chưa? Bạn có bao giờ thắc mắc pt la gì trong hóa học, nếu như bạn có những băn khoăn đó thì hãy đọc ngay bài viết dưới đây sẽ giải đáp một cách tổng quát và đầy đủ nhất cho bạn về pt la gì trong hóa học trên.
PT la gì trong hóa học?
Theo bảng tuần hoàn các nguyên tố hóa học thì PT chính là ký hiệu của Platin hay còn có một tên gọi khác theo Tiếng Việt là bạch kim hay vàng trắng. Số nguyên tử của pt là 78 và cũng nằm ở vị trí số 78 trong bảng tuần hoàn nguyên tố hóa học.

Lịch sử về nguyên tố Platin.
– Tên Platin có nguồn gốc từ thuật ngữ tiếng Tây Ban Nha “platina del Pinto”, nghĩa đen là “sắc hơi óng ánh bạc của sông Pinto”.
– Vào năm 1906, Platin đã được phát hiện trong khu vực Bushveld của Nam Phi ngay sau khi crôm được phát hiện Năm 1865.
– Platin là kim loại chuyển tiếp rất quý hiếm, Platin có màu xám trắng, đặc dẻo, dễ uốn. Mặc dù có sáu đồng vị tự nhiên, nhưng Platin vẫn là một trong những nguyên tố hiếm nhất trong lớp vỏ của Trái Đất với mật độ phân bố tb khoảng 0,005 mg/kg. Pt thường được tìm thấy trong một số quặng niken và đồng, chủ yếu là ở Nam Phi chiếm 80% tổng sản lượng trên toàn thế giới.
– Platin thường xuất hiện trong bồi tích tự nhiên của một số con sông trên thế giới, nó lần đầu tiên được sử dụng để sản xuất các đồ tạo tác bởi người bản xứ Nam Mỹ vào thời kỳ tiền Columbus. Platin từng được nhắc đến trong các bản thảo ở châu Âu vào những năm đầu thế kỷ 16, nhưng nó vẫn không được phổ biến cho đến năm 1748, khi Antonio De Ulloa ra báo cáo về một loại kim loại mới có nguồn gốc từ Colombia, về sau đó Platin đã trở thành tâm điểm của các cuộc điều tra khoa học.

Bạn đang tìm hiểu pt la gì trong hóa học
Tính chất chung:
- Số nguyên tử (số proton có trong hạt nhân): 78
- Vị trí trong bảng tuần hoàn
+ Ô: số 78
+ Nhóm: VIIIB
+ Chu kì: 6
- Ký hiệu nguyên tử Platin (trong bảng tuần hoàn các nguyên tố hóa học): Pt.
- Nguyên tử khối: 195,09 g/mol
- Độ âm điện: 2,28.
- Số oxi hóa là: +2; +3; +4; +5; +6.
- Cấu hình của electron: [Xe] 4f14 5d9 6s1
- Thế điện cực chuẩn (E0Pt2+/Pt ) = 1,2V.
- Phân loại Kim loại chuyển tiếp
- Nhóm, phân lớp 10, d
- Khối lượng nguyên tử (khối lượng trung bình của một nguyên tử): 195,1.
- Mật độ: 21,45 g/cm³.
- Trạng thái vật chất của Platin: chất rắn.
- Nhiệt độ nóng chảy là: 3215,1o F (1768,4o C).
- Nhiệt độ sôi: 6917 F (3825 C).
- Số đồng vị tự nhiên của platin (các Nguyên tử có cùng nguyên tố và khác số Nơtron) là 6. Ngoài ra còn có 37 đồng vị nhân tạo được tạo ra ở trong phòng thí nghiệm.
- Platin tổng có sáu đồng vị tự nhiên: 190Pt, 192Pt, 194Pt, 195Pt, 196Pt, và 198Pt.
- Trong đó phổ biến nhất trong số này là Pt-195 (chiếm 33,83% số lượng tự nhiên) đây là đồng vị ổn định duy nhất có spin khác 0; spin l=½.
- Pt-194 ( chiếm 32,97% số lượng tự nhiên)
- Pt-196 (25,24% số lượng tự nhiên)
- Pt-198 (7,16% số lượng tự nhiên), đồng vị này cũng phân rã alpha, nhưng với chu kỳ bán rã lớn hơn 3,2 × 1014 năm, cho nên nó được coi là ổn định
- PT 192 (0,78% số lượng tự nhiên),
- Pt-190 (0,01% số lượng tự nhiên), đồng vị 190Pt là không ổn định, mặc dù nó bị phân rã với chu kỳ bán rã 6,5 × 1011 năm.
- Platin cũng còn có 31 đồng vị tổng hợp khác nhau, với khối lượng nguyên tử từ 166 đến 202, nâng tổng số đồng vị lên con số 37. Trong số các đồng vị trên, 166Pt là có ít ổn định nhất với chu kỳ bán rã 300 μs, ổn định nhất chính là 193Pt với chu kỳ bán rã lên tới 50 năm. Phần lớn các đồng vị Platin phân rã hạt nhân theo kiểu kết hợp giữa phân rã beta và phân rã alpha. Các đồng vị 188Pt, 191Pt, và 193Pt thông thường phân rã khi bắt electron.190Pt và 198Pt chính là phân rã beta kép.
- Platin tự nhiên thông thường được tìm thấy ở dạng tinh khiết hoặc hợp kim với Iridi như platiniridium. Phần lớn các Platin tự nhiên được tìm thấy ở lớp trầm tích đại trung sinh.
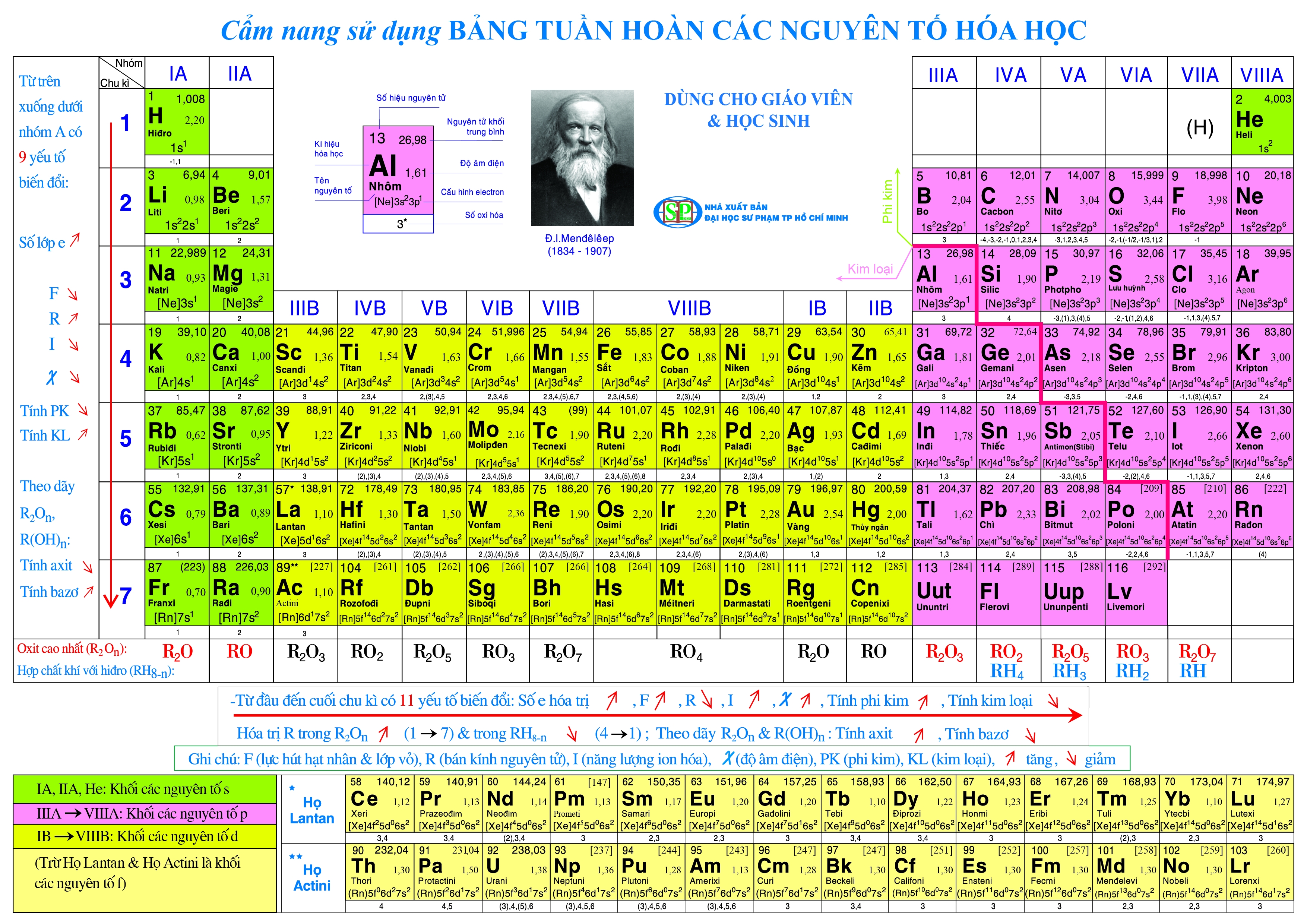
Bảng Tuần Hoàn Hóa Học
Bạn đã hiểu rõ hơn về pt la gì trong hóa học chưa, cùng đọc tiếp xem còn điều gì thú vị về nguyên tố này nhé.
Tính chất vật lí của Platin
– Platin là một kim loại quý, màu trắng – xám, tương đối mềm, rất dễ cán kéo, rèn được, khó nóng chảy.
– Platin có khối lượng riêng là 21,45 g/cm3; nhiệt độ nóng chảy của nó là 1.7720C và nhiệt độ sôi là 3.8000C.
Tính chất hóa học của Platin:
Platin là một kim loại khá kém hoạt động. Platin thuộc nhóm 10 của bảng tuần hoàn vì vậy nó có tính trơ, rất ít khi bị ăn mòn thậm chí ở nhiệt độ cao, vì vậy nó được xem là một kim loại quý. Vậy platin là gì trong hóa học, cùng tìm hiểu các tính chất cơ bản của hợp chất này nhé.
Platin tác dụng với phi kim
Khi nung nóng, Platin tác dụng được với phi kim có tính oxi hóa mạnh (như oxi, halogen,…)
Phương trình ví dụ:
- Pt + O2 → PtO2.
- Pt + Cl2 → PtCl2.
Platin tác dụng với axit
Platin không tan trong axit, nó chỉ tan trong nước cường toan và HCl đặc có bão hòa clo.
Phương trình ví dụ:
- 3Pt + 18HCl (đặc) + 4HNO3 (đặc) → 3H2[PtCl6] + 4NO2 + 8H2O.
- Pt + 2HCl(đặc, nóng) + 2Cl2 → H2[PtCl6]

6. Hợp chất của Platin
Halogen
- Acid Hexachloroplatinic đây có lẽ là hợp chất bạch kim quan trọng nhất, nó tạo nên các hợp chất platin khác. Chính bản thân acid này được ứng dụng nhiều trong nhiếp ảnh, khắc kẽm, mực in không phai, mạ, làm gương, nhuộm màu sứ, và được xem như một chất xúc tác.
- Tác dụng của acid hexachloroplatinic kết hợp với muối amoni, ví dụ như clorua amoni, tạo thành hexachloroplatinate amoni không tan trong dung dịch amoniac. Khi đốt nóng muối amoni này với sự có mặt của hiđro sẽ tạo ra platin nguyên chất.[18] Kali hexachloroplatinate không tan, và acid hexachloroplatinic được sử dụng trong việc xác định ion kali bằng phương pháp phân tích trọng lượng.
- Khi acid hexachloroplatinic được nung nóng, sẽ được phân hủy bằng Pt(IV) clorua và Pt(II) clorua rồi thành các platin nguyên tố theo các bước phản ứng dưới đây:
- (H3O)2PtCl6·nH2O cân bằng với PtCl4 + 2 HCl + (n + 2) H2O
- PtCl4 cân bằng với PtCl2 + Cl2
- PtCl2 cân bằng với Pt + Cl2
Cả ba phản ứng trên đều là phản ứng thuận nghịch. Platin (II) và Platin (IV) bromua cũng đều có những phản ứng tương tự. Platin hexafluoride còn là một chất ôxy hóa mạnh có khả năng oxy hóa cả oxy.
- O2 + PtF6 → O2[PtF6]
Ôxit
- Ôxít Platin(IV), PtO2, còn được gọi chính là chất xúc tác của Adams, một chất bột màu đen hòa tan trong dung dịch KOH và acid đậm đặc. PtO2 và hiếm hơn PtO đều bị phân hủy khi được đun nóng. Ôxit Platin(II,IV), Pt3O4, được hình thành từ những phản ứng sau đây:
2 Pt2+ + Pt4+ + 4 O2− → Pt3O4
Platinum cũng tạo một triôxít với số ôxy hóa +4.
Vậy là chúng ta đã trả lời được pt la gì trong hóa học, cùng xem Platin có những ứng dụng gì trong cuộc sống ở mục tiếp theo nhé.
Ứng dụng của PT trong cuộc sống:
Vậy là chúng ta đã trả lời được pt la gì trong hóa học, cùng xem Platin có những ứng dụng gì trong cuộc sống nhé.
- Platin được sử dụng trong việc làm chất xúc tác, trang thiết bị trong phòng thí nghiệm, thiết bị điện báo, các điện cực, nhiệt kế điện trở bạch kim và thiết bị nha khoa, đồ trang sức.
- Ngoài ra Platin còn là một vật liệu khan hiếm, rất quý và có giá trị bởi vì sản lượng khai thác hằng năm chỉ vỏn vẹn tầm vài trăm tấn.
- Vì Platin là một kim loại nặng, vì thế ảnh hưởng không tốt đối với sức khỏe con người khi tiếp xúc với các muối của nó, nhưng do khả năng chống ăn mòn cho nên có ít độc hại hơn so với các kim loại khác. Ngoài ra một số hợp chất của Platin, đặc biệt là cisplatin, được sử dụng để dùng trong hóa trị liệu chống lại một số loại bệnh ung thư.

So sánh Platinum và Bạc
- Bề ngoài Platinum có vẻ bóng và sáng hơn bạc, trong khi đó bạc lại đục và tối màu hơn.
- Về giá trị thì Platinum đắt hơn rất nhiều so với bạc. Chính vì thế, các trang sức bằng bạc thường được chế tác nhiều phù hợp với xu hướng hiện nay. đây chính là điều mà platinum không có.
- Các sản phẩm bằng bạc trong tiệm trang sức thường được đánh kí hiệu bằng số 925 hoặc S925.
- Ngoài ra Bạc dễ phản ứng trong môi trường có khí độc, và bị xỉn màu. Trong khi đó, platinum lại trơ và vẫn giữ nguyên được vẻ sáng bóng của nó.
Trên đây là toàn bộ những thắc mắc giải đáp cho câu hỏi “pt la gì trong hóa học”. Hi vọng với những kiến thức tổng quan mà chúng tôi cung cấp, bạn đã hiểu rõ hơn về Platin. Hãy lưu bài viết lại để những lúc quên chúng ta lại ôn lại kiến thức nhé. Chúc các bạn học tập và làm việc thật tốt.